Sản xuất thuốc vi phạm chất lượng, Công ty Stallion Laboratories Pvt. Ltd bị xử phạt
Thông tin từ Cục Quản lý dược (Bộ Y tế) cho biết Công ty Stallion Laboratories Pvt. Ltd đã sản xuất thuốc Rabesta 20 (Rabeprazol natri 20mg), Số GĐKLH: VN-18521-14 Số lô: V-159, NSX: 14/02/2022, HD 13/02/2024 vi phạm chất lượng mức độ 2 theo quy định của pháp luật; sản xuất thuốc có thay đổi lớn so với hồ sơ đăng ký thuốc đã được phê duyệt nhưng chưa được phê duyệt nội dung thay đổi theo quy định của pháp luật.
Đối với 2 hành vi vi phạm nêu trên, Công ty Stallion Laboratories Pvt. Ltd bị áp dụng hình thức xử phạt, biện pháp khắc phục hậu quả với tổng số tiền phạt là 120 triệu đồng.
Ngoài xử phạt hành chính, Công ty Stallion Laboratories Pvt. Ltd buộc tiêu hủy toàn bộ số thuốc Rabesta 20 (Rabeprazol natri 20mg), Số GĐKLH: VN-18521-14 Số lô: V-159, NSX: 14/02/2022, HD 13/02/2024 vi phạm chất lượng.
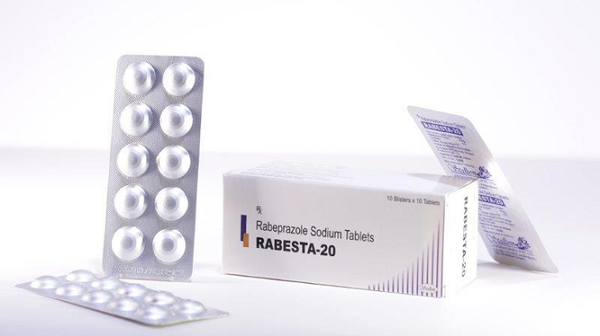
Thuốc Rabesta 20 (Rabeprazol natri 20mg) do Công ty Stallion Laboratories Pvt. Ltd sản xuất.
Theo quyết định xử phạt vi phạm hành chính, Công ty Stallion Laboratories Pvt. Ltd (đại diện chấp hành quyết định xử phạt vi phạm hành chính là Văn phòng đại diện Stallion Laboratories Pvt. Ltd tại TP.HCM) phối hợp với các đơn vị liên quan, thực hiện biện pháp khắc phục hậu quả, báo cáo kết quả thực hiện về Cục Quản lý dược trong vòng 30 ngày kể từ ngày ban hành quyết định.
Quyết định này được giao cho Ông Parmar Dharmesh Maheshbhai, người đại diện của tổ chức chấp hành quyết định xử phạt. Nếu quá thời hạn mà đại diện Công ty Stallion Laboratories Pvt. Ltd không tự nguyện chấp hành sẽ bị cưỡng chế thi hành theo quy định của pháp luật.
Trước đó, ngày 23/12/2022, Cục Quản lý dược có công văn gửi Sở Y tế các địa phương thông báo thu hồi toàn quốc viên nén bao tan trong ruột Rabesta 20 (Rabeprazol natri 20mg) do Stallion Laboratories Pvt. Ltd sản xuất, Công ty cổ phần dược - thiết bị y tế Đà Nẵng (Dapharco) nhập khẩu.
Nguyên nhân thu hồi sản phẩm thuốc được xác định do thuốc không đạt tiêu chuẩn chất lượng về chỉ tiêu độ hòa tan, độ hòa tan trung bình dưới 50% so với tiêu chuẩn chất lượng, vi phạm mức độ 2.
Thanh Thảo















 new_300x250.jpg)